Dermatose Nodulaire Contagieuse de la Vache (DNC): l’Abattage « Inutile » d’Animaux par la France ?
Les contenus de ce site ne peuvent donc pas constituer des provocations à abandonner ou à s’abstenir de suivre un traitement médical thérapeutique ou prophylactique, ni non plus des provocations à adopter des pratiques ayant une finalité thérapeutique ou prophylactique.
Par Hélène Banoun, Jean-François Lesgards et Olivier Frot


Table des matières
Situation actuelle
Le premier cas de Dermatose Nodulaire Contagieuse (DNC) est apparu en Savoie le 29 juin 2025, au 9 août 2025, on recense 71 foyers (37 élevages) dans les deux départements de Savoie.[1], [2]
La vaccination a débuté le 19 juillet dans un rayon de 50 km autour des foyers. A la date du 1er août, 1/3 des 310 000 bovins à vacciner sur le Zone Réglementée (ZR) l’ont été.
La DNC est une pathologie strictement bovine sans risque pour la santé humaine. Une vaccination totale des vaches de la région est en cours comme cela a déjà été pratiqué dans d’autres pays. A ce jour, entre 1500 et 2000 animaux (vaches laitières et destinées à la consommation) ont été abattus sur les 170000 environ, que compte la Savoie.
Règlements UE et décision du gouvernement français
Le droit européen, sous la forme de règlements d’application directe ne nécessitant pas de transposition en droit interne, définit les conduites à tenir par les autorités nationales qui disposent donc d’une liberté limitée et encadrée.

Le règlement 2018/1882 [3] pose certains principes et renvoie au règlement 2016/429 pour les mesures de prévention et d’éradication.
Dans son troisième considérant de préambule, qui indique les intentions du texte, il souligne l’importance de « tenir compte de la gravité potentielle de leur impact sur la santé publique ou animale, l’économie, la santé ou l’environnement ».
L’article premier classifie 5 types de maladies, classifiées de A à E.
L’annexe donne une liste de maladie, dans laquelle on retrouve (page L308/25) la dermatose nodulaire, qui relève de trois catégories à la fois (A+D+E) :
- * Catégorie A : maladies répertoriées qui ne sont habituellement pas présentes dans l’Union et à l’égard desquelles des mesures immédiates d’éradication doivent être prises aussitôt qu’elles sont détectées ;
- * Catégorie D : une maladie répertoriée à l’égard de laquelle des mesures s’imposent en vue d’en empêcher la propagation en cas d’entrée dans l’Union ou de mouvements entre les États membres, telle que visée à l’article 9, paragraphe 1, point d), du règlement (UE) 2016/429 ;
- * Catégorie E : une maladie répertoriée à l’égard de laquelle une surveillance est nécessaire au sein de l’Union, telle que visée à l’article 9, paragraphe 1, point e), du règlement (UE) 2016/429.
Nous sommes donc en présence d’une maladie connue, habituellement non présente en UE et devant faire l’objet d’une éradication immédiate et de mesures à prendre par les États membres.
Le règlement (UE) 2016/429 [4] donne les mesures à prendre
Son article 8-2 dispose que « La Commission établit, au moyen d’actes d’exécution, la liste des espèces visées au paragraphe 3 du présent ». Le §3 renvoie aux « espèces animales ou groupes d’espèces (..) s’ils sont affectés ou s’ils présentent un risque de propagation d’une maladie répertoriée particulière du fait qu’ils : a- sont sensibles à une maladie particulière répertoriée (..) sont des espèces vectrices ou réservoirs de la maladie concernée (…) »
Son article 9-1 précise les dispositions de prévention et de lutte contre ces maladies et renvoie à divers articles du corps de ce même règlement.
L’article 9-2 du même règlement précise que « la Commission précise, au moyen d’actes d’exécution, l’application des mesures de prévention et de lutte visées au paragraphe 1 »
En l’espèce deux décisions d’exécution ont été prises concernant la France, l’une le 03 juillet 2025 [5], non publiée, et une seconde le 20 juillet 2025 [6], également non publiée. Il n’est donc pas possible de savoir ce qui a été décidé par la Commission. En revanche, une décision de même type a été prise pour l’Italie le 27 juin, celle-ci publiée [7]. Cette dernière décision est applicable jusqu’au 10 août 2025 et se limite à préconiser la mise en place d’une zone réglementée de protection et de surveillance, en Sardaigne.
Concernant l’abattage systématique des troupeaux, l’article 61-1-b du règlement 2016/429 prévoit « la mise à mort ou l’abattage des animaux susceptibles d’être contaminés ou de contribuer à la propagation de la maladie répertoriée ». Cette solution se trouve parmi d’autres possibilités dont la liste n’est pas exhaustive. L’article dispose que « l’autorité compétente prend immédiatement une ou plusieurs de mesures suivantes », parmi lesquelles on trouve en effet l’abattage, mais aussi « la vaccination ou le traitement par d’autres médicaments vétérinaires », « l’isolement, la mise en quarantaine » …
En revanche, le RÈGLEMENT DÉLÉGUÉ (UE) 2020/687 DE LA COMMISSION du 17 décembre 2019 complétant le règlement (UE) 2016/429 du Parlement européen et du Conseil en ce qui concerne les règles relatives à la prévention de certaines maladies répertoriées et à la lutte contre celles-ci confère un caractère systématique à l’abattage, dans son article 12 qui dispose que :
« Mesures de lutte contre la maladie en cas de confirmation officielle de l’apparition d’un foyer d’une maladie de catégorie A chez des animaux détenus dans un établissement
- À la suite de la confirmation officielle de l’apparition d’un foyer d’une maladie de catégorie A dans un établissement conformément à l’article 11, l’autorité compétente ordonne, en plus des mesures prévues à l’article 7, l’application immédiate des mesures de lutte contre la maladie suivante sous la supervision de vétérinaires officiels :
tous les animaux des espèces répertoriées détenus dans l’établissement touché sont mis à mort dès que possible sur place, dans l’établissement, d’une manière qui permette d’empêcher tout risque de propagation de l’agent pathogène de la maladie de catégorie A concernée pendant et après la mise à mort (…)”
Ledit règlement prévoit cependant certaines dérogations à l’abattage systématique, dans son article 13 : « 2. L’autorité compétente peut accorder une dérogation à l’article 12, paragraphe 1, point a), aux catégories suivantes d’animaux, sous réserve que les conditions énoncées au paragraphe 3 soient remplies :
a) les animaux détenus dans un établissement fermé ;
b) les animaux détenus à des fins scientifiques ou à des fins liées à la conservation d’espèces protégées ou en danger ;
c) les animaux officiellement enregistrés au préalable en tant que races rares ; et
d) les animaux possédant une valeur génétique, culturelle ou éducative élevée dûment justifiée”.
Le problème réside dans la classification de la DNC en catégorie A+D+E par le règlement (UE) 2018/1882 de la Commission du 03 décembre 2018 sur l’application de certaines dispositions en matière de prévention et de lutte contre les maladies à des catégories de maladies répertoriées et établissant une liste des espèces et des groupes d’espèces qui présentent un risque considérable du point de vue de la propagation de ces maladies répertoriées, alors que cette maladie est de nature bénigne, n’est pas transmissible à l’homme et n’affecte pas la qualité de la viande ni celle du lait. Par suite, les règles particulièrement strictes prévues pour les maladies de catégorie A vont s’appliquer à la DNC.
Le règlement précité donne dans son article premier-1 la définition des maladies de catégorie A :
« «maladie de catégorie A»: une maladie répertoriée qui ne sont habituellement pas présentes dans l’Union et à l’égard desquelles des mesures d’éradication immédiates doivent être prises aussitôt qu’elles sont détectées, telle que visée à l’article 9, paragraphe 1, point a), du règlement (UE) 2016/429 ».
Ainsi, le seul critère choisi par ce texte concerne non pas la gravité ou ses conséquences, ni même l’existence de traitements, mais, comme dispose le règlement 2016/429, article 9, paragraphe 1, point a) :
« en ce qui concerne les maladies répertoriées qui ne sont habituellement pas présentes dans l’Union et à l’égard desquelles des mesures d’éradication immédiates doivent être prises aussitôt qu’elles sont détectées, les dispositions suivantes s’appliquent, le cas échéant :
i) les dispositions concernant la sensibilisation et la préparation à la maladie visées dans la partie III, titre I (articles 43 à 52) ;
ii) les mesures de lutte contre les maladies prévues dans la partie III, titre II, chapitre 1 (articles 53 à 71) ; et
iii) les dispositions concernant l’établissement de compartiments prévues à l’article 37, paragraphe 1.
Pour ces maladies répertoriées, les mesures visées au point b), en tant que de besoin, ainsi qu’aux points d) et e) s’appliquent également, selon le cas ».

L’abattage de tous les animaux sensibles qui ont été exposés à l’infection, ou au moins de ceux qui présentent des signes cliniques, est une mesure de contrôle de la maladie généralement recommandée (Tuppurainen E and Galon N, 2016). Il faut noter que d’après Eom HJ et al. (2023), la Turquie et Israël ont pratiqué l’abattage total des troupeaux infectés mais cela n’a pas empêché la maladie de revenir (Eom HJ et al., 2023).
Dans les faits : Euthanasie et Vaccination de Masse
La vaccination des troupeaux de la Zone Réglementée débutée le 18 juillet se poursuit. A la date du 31 juillet, 1/3 des 310 000 bovins à vacciner sur la ZR l’ont été.
Cette politique stricte a été validée par le Ministère de l’Agriculture et de la Souveraineté Alimentaire (Comité national d’orientation de la politique sanitaire animale et végétale, CNOPSAV 2025) et de différents acteurs.
À l’issue des concertations du CNOPSAV, et sur la base des présentations techniques d’organismes tels que l’ANSES, le CIRAD, le CNOV, la FSVF, le SNVEL, la SNGTV, la DGAL et le CGAAER, une stratégie nationale de lutte contre la dermatose nodulaire contagieuse a été adoptée quasi unanimement. Elle repose sur trois axes principaux :
(i) l’abattage total des animaux au sein de chaque unité épidémiologique infectée, conformément aux obligations européennes de lutte contre les maladies animales de catégorie A ;
(ii) la délimitation de zones réglementées, avec mise en œuvre de mesures strictes de surveillance, de biosécurité et de restriction des mouvements ;
(iii) le lancement d’une campagne vaccinale obligatoire dans ces zones ciblées.
Un dispositif d’accompagnement individualisé est également prévu pour les éleveurs concernés, incluant des indemnisations financières et un soutien psychologique.
Si on veut se « rassurer », ce n’est « que » environ 1% du cheptel de la Savoie qui a été abattu, et la France compte un nombre très important d’exploitations et encore 16 millions de bovins, comme le montre la figure ci-dessous.
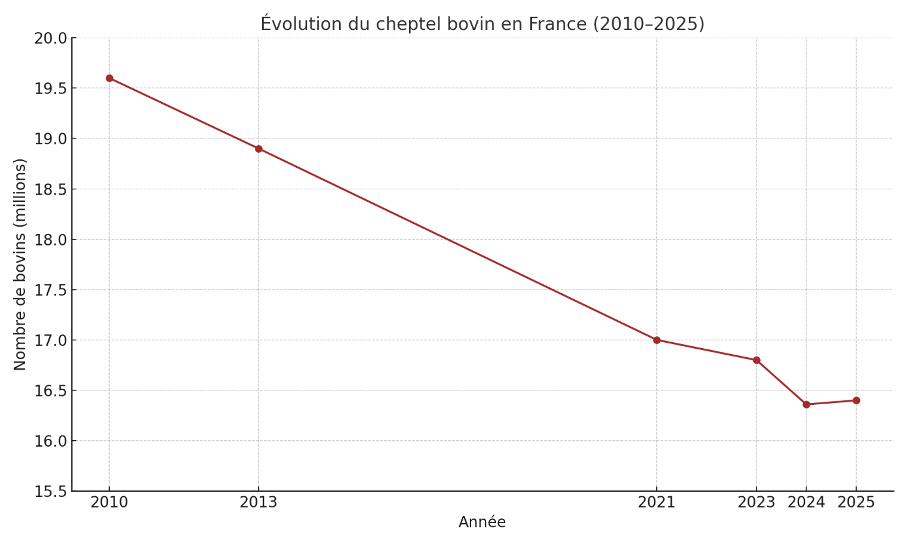
Voici le graphique montrant l’évolution du cheptel bovin en France entre 2010 et 2025. On observe une baisse continue du nombre de bovins, passant d’environ 19,6 millions en 2010 à 16,4 millions estimés en 2025.
Entre 2024 et 2025, le cheptel bovin français se maintient autour de 16,5 millions de têtes, bien que la tendance à la baisse persiste. Cette contraction reprend son rythme moyen observé entre 2016 et 2022, avec une diminution annuelle d’environ 2,2 %, après un ralentissement relatif en 2023 (–1,1 %). Globalement, depuis le début du processus de décapitalisation engagé en 2017, la France a perdu près de 2,9 millions de bovins, soit une réduction de 15,2 % de son cheptel par rapport à 2016.[8]
Mais il est particulièrement choquant et préoccupant que la détection d’un seul bovin positif à la dermatose nodulaire contagieuse (DNC), même en l’absence de signes cliniques évocateurs chez l’animal ou ses congénères, entraîne systématiquement l’abattage de l’ensemble du troupeau concerné, conformément aux mesures sanitaires en vigueur visant à enrayer rapidement la propagation virale.
Selon les protocoles en vigueur, les animaux doivent être sédatés par injection intraveineuse ou intramusculaire (Xylazine à 0,3 mg/kg par voie IM ou 0.1 mg/kg voie IV; ou Détomédine, 10 – 20 microgramme/kg IM ou IV ; ou Kétamine à 0,1 mg/kg IV Xylazine puis 2mg/kg IV Kétamine) puis euthanasiés par intraveineuse (Euthasol vet. Solution injectable/Pentobarbital sous forme de sel de sodium IV, IC Si IV à 0,35 ml/kg ou T 61 [Embutramide, Mébézonium sous forme de diiodure et Tétracaïne sous forme de chlorhydrate IV 4 – 6 ml/50kg]). [9]

Vidéo témoignage sur le réseau X, de l’euthanasie des vaches en Savoie [10]

Mieux connaître la Dermatose Nodulaire Contagieuse (DNC) ou Dermatose Bovine
Maladie et symptômes de la DNC
Cette pathologie virale est strictement spécifique aux bovins domestiques (Bos Taurus) comme nos bovins, aux zébus (Bos indicus) et aux buffles d’eau (Bubalus bubalis), bien qu’elle ait occasionnellement été observée chez certaines espèces de ruminants sauvages. Elle n’est pas transmissible à l’Homme.
La dermatose nodulaire contagieuse (DNC), ou Lumpy Skin Disease en anglais (LSD), a une incubation naturelle de 2 à 5 semaines, plus courte en conditions expérimentales (7–14 jours) (Wolff et al., 2020). Elle peut se présenter sous forme chronique, subaiguë ou aiguë, débutant par une fièvre pouvant atteindre 41 °C (température normale 38°C) suivie d’un amaigrissement, d’un écoulement oculaire et d’une chute de lactation. Des nodules douloureux apparaissent ensuite sur différentes zones cutanées (museau, pattes, scrotum, etc.) (Datten et al., 2023) (Pandey et al., 2022). Dans les cas graves, plus de 100 nodules peuvent couvrir le corps, évoluant en vésicules, croûtes puis lésions nécrotiques (Kumar et al., 2021). Cela provoque une gêne locomotrice et des complications comme septicémie, pneumonie, avortement ou infertilité. La guérison est lente, souvent entravée par des infections secondaires, des mastites et des attaques de mouches (Murti et al., 2024).
Le taux de mortalité est relativement faible (généralement 1 à 5 %), mais peut atteindre jusqu’à 40 % chez les animaux jeunes (Friedrich-Loeffler-Institut 2025) et le taux de morbidité (fait de développer la maladie et les symptômes) est normalement située entre 10 et 20 % et varie de 3 à 85 % dans le monde entier (Akther M et al., 2023). L’infection endommage les peaux et affecte la production de viande bovine et de lait, ce qui a des répercussions sur le commerce d’exportation (Asset UK, 2025).
Le taux de morbidité pourrait être lié à la race. Toutes les races n’ont pas la même sensibilité à la maladie : La sensibilité des bovins à la LSDV est influencée par divers facteurs, notamment la race, l’âge et le statut immunitaire en Afrique ont montré que certaines races bovines indigènes sont moins exposées au LSD que les bovins exotiques ou croisés (Kumar et al., 2025).
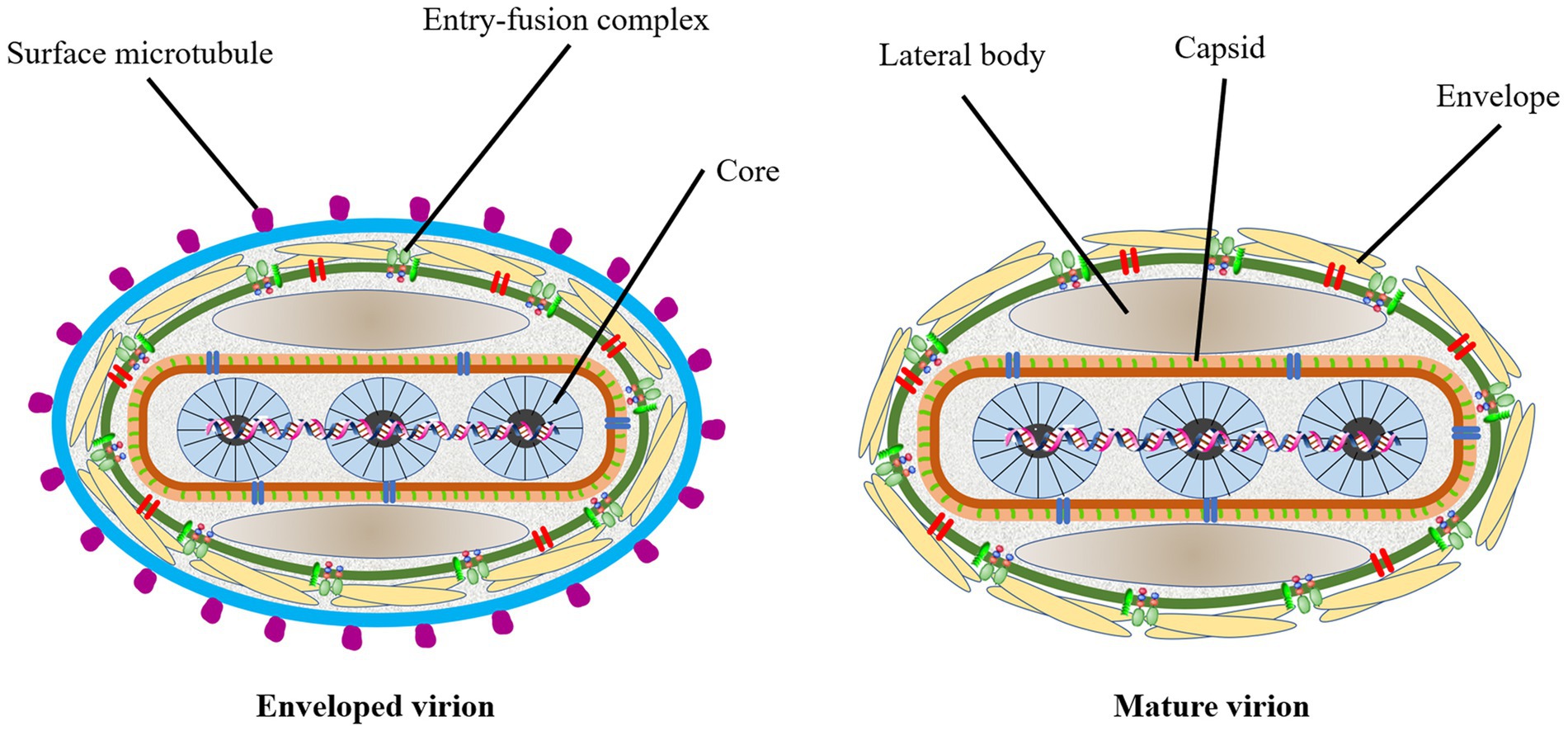
Image Liang et al, 2022
Etiologie (cause et facteurs de la maladie)
Le virus responsable de la dermatose nodulaire contagieuse (DNC) appartient à la famille des Poxviridae, genre Capripoxvirus (CaPV), et possède un génome ADN double brin d’environ 151 kpb. Il est de forme ovale (230–260 nm), enveloppé, et se réplique dans le cytoplasme (intérieur des cellules). Il comporte 156 gènes, dont 146 codent pour des protéines conservées impliquées dans la réplication, la virulence et la transcription. Il est stable entre pH 6,6–8,6 et résiste dans l’environnement jusqu’à 6 mois selon les conditions (tissu protégé du soleil). Il est inactivé à 55 °C en 2 heures ou 65 °C en 30 minutes. Il est sensible à des désinfectants comme l’iode dilué, le formol 1 %, l’hypochlorite de sodium, les solvants lipidiques, et les UV à 55 °C.
Le virus de la dermatose nodulaire contagieuse (LSDV pour Lumpy Skin Disease Virus) présente une stabilité notable dans l’environnement, pouvant rester infectieux jusqu’à 35 jours au sein des lésions cutanées. Il est éliminé par divers fluides biologiques, notamment les sécrétions nasales, lacrymales, le lait (jusqu’à 11 jours) et le sperme (jusqu’à 22 jours). En revanche, aucune donnée ne suggère la présence du virus dans les tissus musculaires consommables des animaux infectés. Les virus de la variole ovine et caprine, SPPV et GTPV, dont les nouveaux noms sont C. sheeppox et C. goatpox, appartiennent au même genre que le LSDV, et les séquences génomiques de ces deux virus sont identiques à 97 % à celles du LSDV (Bhakha et al., 2025).
Historique de la maladie et arrivée en France
- 1929–1948 : Premiers cas décrits comme « pseudo-urticaire » en Zambie (ex-Rhodésie du Nord), avec une extension au Zimbabwe, Botswana, Afrique du Sud et Mozambique.
- 1944 : Premiers cas en Afrique du Sud
- 1949–1968 : La maladie atteint l’Angola, le Zaïre, Madagascar, l’Afrique de l’Est (Namibie, Tanzanie, Ouganda, Kenya).
- 1969–1988 : Recrudescence au Soudan et diffusion vers le Tchad, le Niger, le Nigeria, l’Éthiopie, la Somalie, le Cameroun.
- 1989–2008 : Extension hors de l’Afrique subsaharienne, vers l’Égypte, le Moyen-Orient (Israël, Oman, Koweït, Yémen, Émirats, Bahreïn).
- 2009 – aujourd’hui : Propagation en Arabie Saoudite, Irak, Turquie (première fois hors d’Afrique), Iran, Azerbaïdjan. Extension en Europe de l’Est (Grèce, Russie, Balkans) et Asie (Afghanistan, Indonésie).
En Indonésie, premiers cas dans la province de Riau, avec extension à d’autres régions.
Depuis sa première apparition hors d’Afrique en Égypte (1988) et en Israël (1989), la DNC s’est étendue progressivement vers le Moyen-Orient, l’Europe de l’Est et l’Asie (Banoun H et Lesgards JF, 2025) (Akther M et al., 2023) (Eom HJ et al., 2023) (FLI, 2025). Devenue endémique en Turquie dès 2013, elle a atteint la Russie (2015), les Balkans (2016), et l’Asie du Sud à partir de 2019. En 2023, Israël a signalé de nouveaux cas, majoritairement liés à des insectes vecteurs, sans abattage systématique. En 2024, la Tunisie et l’Algérie ont détecté les premiers foyers en Afrique du Nord (EFSA 2024). À l’été 2025, la maladie atteint la Sardaigne, l’Italie du Nord et la France (Savoie), entraînant des restrictions d’exportation vers le Royaume-Uni.
Tests de détection de la maladie
Le diagnostic de la DNC repose d’abord sur les signes cliniques typiques, mais doit être confirmé par des tests de laboratoire. Plusieurs méthodes sont utilisées : culture cellulaire, immuno-histochimie, ELISA, PCR classique et en temps réel, ainsi que l’épreuve de séroneutralisation (SNT), qui est la méthode sérologique de référence malgré sa lenteur (Amin et al., 2021) (Elhaig et al., 2017). Certains tests ne permettent pas de distinguer le LSDV des autres espèces de Capripoxvirus, le test ELISA ne peut pas différencier les anticorps contre le LSDV, le SPPV et le GTPV dans le sérum et le plasma (Akther M et al., 2023).
Les anticorps anti-LSDV ne sont pas des corrélats fiables de la protection. Dans les cas où les anticorps anti-LSDV sont indétectables, l’immunité à médiation cellulaire joue un rôle protecteur crucial (Kumar et al., 2025).
Le virus peut être isolé sur divers types de cultures cellulaires animales. Toutefois, la SNT, bien que très spécifique (97 %), est peu sensible (78 %) et un résultat négatif ne signifie pas toujours absence d’infection. Le western-blot est fiable mais coûteux. Le diagnostic différentiel est essentiel car de nombreuses maladies présentent des symptômes similaires (pseudovariole, fièvre catarrhale, photosensibilisation, tuberculose, etc.), nécessitant un diagnostic vétérinaire rigoureux pour éviter les confusions. La microscopie électronique peut être utilisée pour identifier le virion du poxvirus classique, mais ne peut pas le différencier au niveau du genre ou de l’espèce. Le séquençage (partiel ou du génome entier) fournit le plus d’informations concernant le regroupement en clusters (souches de terrain classiques, de type vaccinal ou, plus récemment, recombinantes de terrain).
Le virus de la DNC [ le LSDV ] se divise en deux clusters principaux: la souche vaccinale Neethling atténuée (1.1) et les souches sauvages (1.2). Depuis 2017, des souches recombinantes issues de recombinaisons entre souches vaccinales et sauvages ont été identifiées, notamment en Asie, possiblement liées à des contaminations par des vaccins (souches 2.1 à 2.5) (Banoun et Lesgards, 2025). Le test DIVA-PCR classique, utilisé pour différencier animaux vaccinés et infectés, devient inefficace face à ces recombinants. Un nouveau test DIVA (Haegeman et al., 2023a) et une méthode HRM post-PCR (Bhakha, 2025) ont été développés pour mieux distinguer souches sauvages, vaccinales et recombinantes. Ce dernier test HRM permet, pour la première fois, une différenciation précise des trois groupes de LSDV, facilitant le suivi épidémiologique. Enfin, il est essentiel de bien différencier LSDV des virus proches comme SPPV et GTPV.
Image wikipedia : Mouche charboneuse Stomoxys calcitrans.
Par User:Fir0002 — Originally uploaded at 09:45, 12 July 2007 as Image:Musca domestica on aloe vera.jpg (was originally misidentified as a house fly, Musca domestica)., GFDL 1.2,
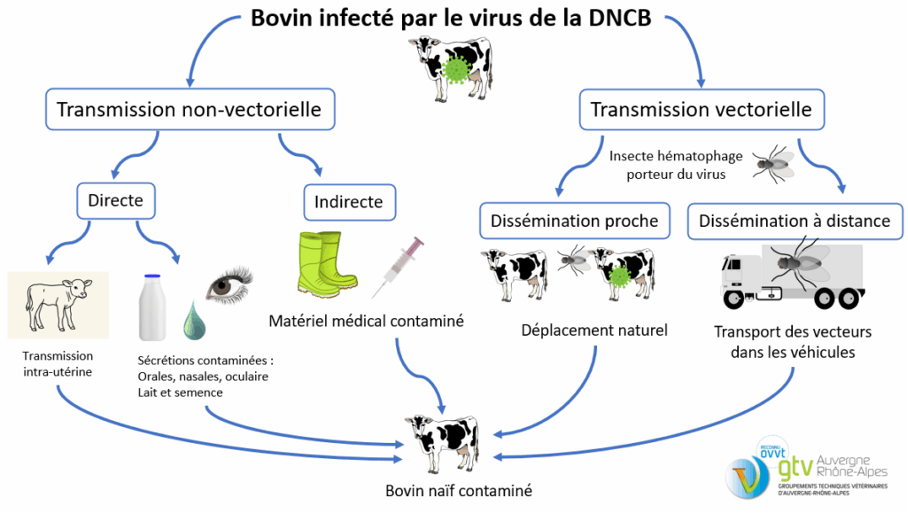
Mode de transmission
Plusieurs hypothèses circulent quant à l’introduction en France : transmission via insectes hématophages depuis l’Italie ou le Maghreb, ou importation de bovins infectés. L’ANSES et l’EFSA recommandaient depuis 2017 de surveiller les semences et mouvements d’animaux, en raison d’un risque (estimé comme « faible à très faible » en 2017) identifié pour la France. Enfin, une confusion a été notée entre des cas de variole ovine en Grèce et la DNC chez les moutons (voir Banoun et Lesgards, 2025).
Source : https://gtvbfc.com/
La maladie aurait pu être introduite en Italie depuis les Balkans, puis diffusée en France, mais cette hypothèse reste peu probable car les Balkans étaient exempts depuis 2017. La transmission via insectes vecteurs depuis le Maghreb ou l’Italie est privilégiée, avec aussi la possibilité d’un bovin importé d’Italie avant les restrictions (atteint de maladie subclinique). Les importations d’animaux vivants et de matériel génétique depuis les Balkans et l’Italie sont faibles, rendant ces voies moins probables. La surveillance accrue des mouvements d’animaux et semences est recommandée. Le risque de contamination est jugé élevé dans plusieurs pays européens à cause des mouvements de bétail et de vecteurs.
L’ANSES, dans son rapport de 2017, recommande d’approfondir les connaissances sur les vecteurs de la dermatose nodulaire contagieuse (DNC), notamment les mouches Stomoxys, taons et tiques, en étudiant leur rôle épidémiologique, la dose infectieuse, le temps de survie du virus dans ces insectes et les modes de transmission (mécanique ou biologique) (ANSES, 2017). L’effet de leur salive sur la transmission doit également être exploré, ainsi que les densités vectorielles et les méthodes de lutte (insecticides, pièges, répulsifs, parasitoïdes). Selon Shridhar, il faut restreindre les mouvements d’animaux, abattre les animaux atteints et vacciner, il n’existe actuellement aucune preuve de l’efficacité de la lutte contre les vecteurs dans la prévention de la maladie (Shridhar ND, 2022).
Concernant l’introduction de la maladie en Italie et en France, l’explication officielle est par insectes vecteurs qui est la voie de transmission la plus courante selon les experts (Haegeman et al, 2023b) (Kumar et al., 2025). Les mouches d’étables (Stomoxys calcitrans) peuvent parcourir jusqu’à 225 km portées par le vent (Showler AT et Osbrink WL, 2015).
Ces insectes sont des vecteurs mécaniques, c’est-à-dire sans multiplication du virus dans le vecteur ; la transmission par contact direct entre animaux est peu courante mais possible (Sanz-Bernardo et al., 2022). Les animaux excrètent le virus dans les écoulements nasaux, les fèces, le sperme et le lait (Kumar et al., 2025). Les insectes nourris sur les lésions cutanées des nodules sont les plus susceptibles de transmettre le virus qui persiste jusqu’à 9 jours sur les pièces buccales. Ce sont plutôt les animaux qui développent des lésions qui vont transmettre le virus.
Les moustiques conservent le virus jusqu’à 14 jours (Kumar et al., 2025)
La transmission de la maladie par les animaux atteints de façon subclinique (pas de nodule mais un écoulement nasal) ou asymptomatique semble peu fréquente mais pas impossible (Haegeman et al., 2023b) (Kumar et al., 2025) et l’importation par matériel génétique est peu probable : la France importe des semences bovines et, marginalement, des embryons depuis l’Italie (et en volumes très faibles depuis les Balkans).
La Vaccination et le Plan de Vaccination contre la DNC
La vaccination peut stimuler l’immunité humorale de l’animal et assurer une protection pendant plus de 7-11 mois, de sorte qu’un calendrier de vaccination annuel avec une dose de rappel est recommandé en raison de la durée inconnue de l’immunité cellulaire et humorale (injection sous-cutanée unique de 2ml). Le vaccin contre la souche sud-africaine Neethling est le vaccin le plus couramment utilisé dans les pays endémiques pour protéger le bétail contre la LSD ; c’est celui qui a été choisi en France (laboratoire OBP, Afrique du Sud ; vaccin vivant atténué homologue = souche identique à celle qui provoque la maladie).
Il s’est avéré efficace comme validé dans les Balkans, où il a contribué de façon déterminante à endiguer la maladie, mais il peut avoir des effets indésirables (Shridhar NB, 2022) (Tuppurainen et al., 2021). L’acquisition d’une immunité efficace est atteinte après 21 jours post vaccination.
Effets indésirables possibles : (fréquence faible : 64 cas déclarés/ 420 000 vaccinations dans les Balkans)
- * Hyperthermie et abattement
- * Baisse de production temporaire
- * Apparition de nodules pouvant mimer la maladie mais disparaissant spontanément en une à deux semaines (un test permet de différencier ces effets secondaires de la maladie)
- * Avortement (rare – conséquence du stress et de l’intervention)
Plusieurs travaux ont mis en évidence la détection de virus vaccinaux dans les nodules cutanés, le sang ou le lait de bovins ayant reçu des vaccins homologues de type Neethling (Shridhar NB, 2022). Il faut environ deux à trois semaines pour qu’une immunité protectrice complète s’établisse après la vaccination, d’où la nécessité de n’inoculer que des animaux sains. En effet, la vaccination d’un animal déjà infecté peut aggraver la maladie et favoriser l’émergence de virus recombinants entre souches vaccinale et sauvage (Akther M et al., 2023). Les lésions cutanées liées au vaccin sont en général plus petites et distinctes de celles provoquées par les souches virulentes de terrain (Shridhar NB, 2022).
Seuls les animaux en bonne santé doivent être vaccinés. La vaccination d’animaux déjà infectés provoque une maladie plus grave et une recombinaison éventuelle entre le virus vaccinal et le virus sauvage (Shridhar NB, 2022).
Le LSDV est un poxvirus, de la même famille que celui de la variole humaine (éradiquée en 1979). La vaccination en période d’épidémie de variole humaine a donné des résultats très contestables par le passé. Un article de 1928 publié dans le BMJ compare le taux de létalité de la variole chez les vaccinés et les non-vaccinés. Chaque année entre 1923 et 1926 le taux de létalité chez les plus de 15 ans était plus élevé chez les vaccinés. Le taux était de 0,3% chez les vaccinés et de 0,06% chez les non vaccinés. Il s’agissait à cette époque de variole peu grave « mild smallpox » (Garrow 1928). Il semble que la vaccination ait eu lieu pendant une épidémie de variole comme ce qui était pratiqué pendant toutes les épidémies en Angleterre. Cinquante pour cent des encéphalopathies se produisaient chez des adultes revaccinés lors d’une épidémie ; la revaccination par un virus vivant en présence du virus sauvage peut donc être rendue responsable d’une maladie plus grave ; la durée de protection conférée par la vaccination est de quelques années (CDC octobre 2024, [11]). L’auteur de cet article de 1964 (Bonaccorsi A et al., 1964) affirme que la vaccination en pleine épidémie est une mesure de panique et doit être condamnée. C’est ce qu’expliquait également en 1889 Alfred R Wallace, le co-auteur de la théorie de l’Évolution (Wallace 1889). Par ailleurs, dans des modèles animaux, aucun avantage significatif de survie à la vaccination post-exposition a été observée à l’aide de modèles d’infection soit MPXV (monkeypox virus) chez les singes ou VACV (virus de la vaccine) chez la souris (Samuelsson, 2008).
Aucun vaccin n’a d’AMM (autorisation de mise sur le marché) en Europe. Le choix de la souche Neethling comme souche vaccinale semble être la seule option disponible pour le moment (ANSES, 2017). Les vaccins utilisés au sein de l’UE seraient : le Lumpy Skin Disease Vaccine for Cattle® d’Onderstepoort Biological Products, (OBP), Afrique du Sud (souche Neethling6), et le Lumpyvax® – MSD Santé Animale, Afrique du Sud (souche de terrain atténuée, type SIS7).(ANSES 2017). Il n’est pas certain que le vaccin provenant d’Afrique du Sud soit la souche Neethling (Tuppurainen, 2021).
Lorsqu’un foyer de DNC est en cours et que des campagnes de vaccination de masse sont menées rapidement, la vaccination d’animaux déjà infectés peut accroître le risque de recombinaison entre des souches du vaccin et des souches de terrain (Shridhar NB, 2022) (Akther M et al., 2023).
Pour information, il faut savoir que des chercheurs travaillent sur des vaccins contre le sida (gp120) avec comme vecteur, le virus de la dermatose nodulaire (poxvirus). [Références des articles et brevets [12] ]
Les traitements
Même si les autorités sanitaires ne reconnaissent pas officiellement de traitements efficaces de la DNC, (dermatose nodulaire, non toxique pour l’homme), différents vétérinaires / scientifiques ont montré qu’il existait des traitements permettant d’améliorer voire de soigner complètement des bovins malades.
En 14 jours avec Ivermectine et antibiotiques par exemple, avec rémission totale et sans lésions (Smriti S et al., 2023).[13]

Animal avant et puis 14 jours après traitement
Autre traitement efficace sur le veau contre la dermatose, guérison en 21 jours :
- – Gentamicin 5 mg/kg poids corp. Injection en Intramusculaire
- – Meloxicum 0.2mg/kg IM
- – Antihistaminique
- – Pansement multivitamines & antiseptique (Halder B et al., 2022) [14].
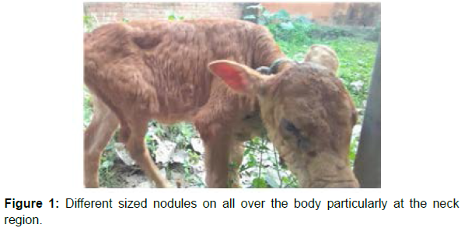
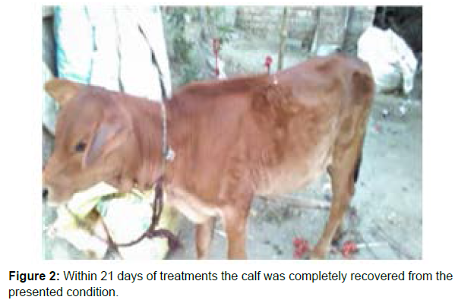
Animal avant et puis 21 jours après traitement
Différents soins peuvent être aussi efficacement apportés aux animaux pour les soulager comme l’utilisation de gel de Diclofénac dans la région œdémateuse et l’application de sulfamide sur les lésions nodulaires (Paul AK, 2020). Feyisa (2018) a également montré que la thérapie combinée de dexaméthasone et d’antibiotiques à large spectre pendant trois jours était efficace contre l’infection par le virus du LSD (Feyisa AF, 2018).
Il serait tout à fait possible en parallèle de la vaccination des bêtes non infectées, de tester ces traitements sur les bêtes malades qui seraient isolées. Une large partie du cheptel pourrait être sauvée. Une interdiction de soigner [comme contre le COVID] n’a aucun sens et n’est pas éthique.
Prévention de la Propagation : Que penser de cette façon « française » de gérer la crise ?
L’Union européenne recommande mais n’impose pas l’abattage total des troupeaux atteints de dermatose nodulaire contagieuse (DNC) ; cette mesure doit être adaptée à chaque situation épidémiologique (UE 2012, UE 2016) (Akther M et al., 2023) (Tuppurainen E et al., 2021). La version actualisée de 2023 précise que « l’autorité compétente peut ordonner la mise à mort préventive » si nécessaire (UE 2023).
Bien que l’abattage immédiat puisse limiter la propagation, son efficacité est compromise par l’incubation silencieuse du virus et ses conséquences socio-économiques (Tuppurainen E and Galon N, 2016). L’abattage ciblé des animaux symptomatiques ou exposés reste recommandé. Toutefois, l’expérience turque et israélienne montre que l’abattage seul ne suffit pas sans vaccination complète et contrôle strict des mouvements (Eom et al., 2023) (EFSA 2020).
En Israël, l’abattage n’est motivé que par le bien-être animal (EFSA 2016, 2020). L’OMSA (ex-OIE) privilégie une stratégie de biosécurité, vaccination massive et contrôle des déplacements, sans mentionner l’abattage (OMSA-WHOA, 2025). Pour l’ANSES, l’abattage et les restrictions de transport sont utiles mais insuffisants (ANSES 2017). Plusieurs spécialistes insistent sur la combinaison vaccination + abattage ciblé, soulignant que la lutte antivectorielle n’a pas démontré d’efficacité (Shridhar NB, 2022).
Lors de l’épidémie de 2016-2017 en Hongrie aucun abattage n’avait été pratiqué et le groupe d’experts avait donné les justifications suivantes : cette mesure d »abattage s’étant montrée inefficace dans d’autres États membres, la létalité de la maladie étant habituellement faible (1-5%), étant donné qu’il n’y avait pas de porteur sain, cela aurait représenté des dommages économiques inutiles pour les propriétaires d’animaux et enfin, l’opinion publique était défavorable à la politique d’abattage (Standing Group of Experts on Lumpy Skin Disease in Europe, 2017).
Lors de l’épidémie de 2016-2017 dans les Balkans, la Grèce a abattu 16% et la Bulgarie 96% des troupeaux contaminés (Tuppurainen ESM et al., 2020) ; aucun de ces 2 pays n’a connu de résurgence de la maladie depuis (UE Webinar, 2025).
Malgré les affirmations officielles, en Italie, la réponse des autorités ne semble pas être l’abattage total : en Sardaigne 2376 vaches composent les troupeaux touchés et 200 animaux ont été abattus ; en Lombardie les 291 animaux du foyer unique ont été abattus. Donc sur un total de 2667 vaches composant les troupeaux atteints, 491, soit 18% des animaux ont été abattus, selon les données officielles au 30 juillet 2025 (Sistema Informativo Veterinario – Bollettino Epidemiologico [15]).
Selon le magazine « Nos Alpes », au 4 août 2025, en Sardaigne, dans la province d’Oristano, 292 bovins malades avaient été recensés, 72 morts et 517 abattus.
En conclusion, les textes européens manquent d’harmonisation, et la majorité des experts privilégient une stratégie intégrant surveillance, restriction des mouvements et vaccination, plutôt que l’abattage systématique des animaux sains.
De plus, en France, il existe des lois contre les « sévices graves ou le fait de commettre un acte de cruauté envers un animal domestique, ou apprivoisé, ou tenu en captivité » passible de 3 ans de prison et 45 000 euros d’amende d’après l’Article 521-1 code pénal.
Aspect économique
La dermatose nodulaire exerce actuellement un impact économique considérable sur l’industrie de l’élevage, car la maladie élimine les petits exploitants marginaux. La dermatose nodulaire est considérée comme une maladie transfrontalière importante. Le transport légal ou illégal d’animaux domestiques et sauvages vivants, y compris leurs produits (lait, viande, peaux et biomatériaux tels que l’embryon, le sperme, le sang et les os), constitue une menace pour la transmission de la DNC à court et à long terme. Le risque de contamination par la DNC était considéré comme élevé en 2021 en Allemagne et en France, ainsi que dans certains pays déjà infectés, comme la Turquie, en raison des mouvements de bétail ou de vecteurs susceptibles de transmettre la DNC (Tuppurainen E et al., 2021).
L’ANSES annonçait un risque très faible pour la France en 2017 (Anses 2017).
À la suite de l’épidémie en France, les exportations vers le Royaume Uni d’animaux vivants, de matériel génétique (sperme, ovule, embryon), de lait cru, de produits laitiers non pasteurisés, les cuirs et peaux (sauf traitement spécial), les sous-produits bovins, sont suspendus en cet été 2025 (Guidance UK)
Les scientifiques britanniques craignaient déjà une contamination européenne en provenance d’Afrique du Nord en passant par l’Espagne (Asset UK, 2025).
Enjeu économique de la filière bovine d’exportation d’animaux vivants de France vers Italie
La France exporte des broutards (jeunes bovins destinés à l’engraissement) vers l’Italie et le pourtour méditerranéen ainsi que du matériel génétique (semences, embryons). La France exporte également des produits transformés (viande, plats préparés, laitages, cuirs, etc..). Ces exportations sont très sensibles aux crises sanitaires qui entraînent des restrictions de mouvement.
Lorsqu’une zone ou un État est déclaré contaminé par la dermatose nodulaire, les bovins ne peuvent plus être exportés vers un État membre sauf dérogation (quarantaine et PCR négatives). De même les animaux vaccinés provenant d’une zone non indemne (ou d’une zone où la vaccination est pratiquée) ne peuvent pas être déplacés vers une zone ou un État membre indemne sans vaccination, sauf dans des cas très spécifiques. Pour récupérer le statut de zone ou d’État indemne, il faut 2 à 3 ans après la fin de la vaccination avec l’absence prouvée de la maladie. Selon le GDS69, la durée d’interdiction après le dernier vaccin ne serait que de 14 mois.
Ces contraintes économiques expliquent en partie les décisions des autorités d’abattage total et de vaccination limitée aux zones touchées afin de contenir la maladie et de sauvegarder les capacités d’exportation des bovins français vivants.
Dans cette logique de conserver à la France le statut de région indemne (qui ne s’applique que si aucun cas n’est recensé ni aucune vaccination entreprise), l’État refuse la vaccination aux éleveurs Corses qui la demandent en raison de la proximité avec la Sardaigne .
Questions et Discussion
Sur la vaccination
La vaccination est une solution à moyen terme mais elle est incapable d’éradiquer la maladie.
Selon les fabricants de vaccins Sud-Africains (Hunter P and Wallace D, 2001) , la DNC a été absente dans leur pays entre les années 1960 et les années 1990 (la première épidémie y a eu lieu en 1944). Le vaccin a été introduit en 1984 et a été injecté massivement à partir des années 1990, tout en ne couvrant toutefois que 20% du bétail. La vaccination échouerait sur 1/10 animal qui ne séroconvertit pas. L’immunité vaccinale est de courte durée et nécessite des rappels annuels, l’immunité maternelle transmise au veau dure 6 mois environ (seulement 2 mois selon certains chercheurs (Kumar et al., 2025). La vaccination en période épidémique arrive trop tard pour protéger les animaux. La maladie reste endémique et elle apparaît maintenant toute l’année (et pas seulement pendant la saison chaude où les insectes vecteurs sont les plus présents).
Bien que la Géorgie ait commencé à vacciner le bétail en 2014 après une épidémie dans l’Azerbaïdjan voisin, une épidémie a été documentée en 2016 et est réapparue en 2018 avec six autres foyers (Zeynalova et al., 2016).
D’un point de vue économique il est impossible de laisser se développer la maladie afin que les troupeaux domestiques acquièrent une immunité naturelle mais ce serait pourtant la solution à long terme (la faune sauvage sensible en Afrique (et donc immunisée depuis longtemps est insensible à la maladie (Hunter P and Wallace D, 2001).
Résumé de la déclaration du secrétaire général du syndicat agricole de la Coordination Rurale : Il regrette que des troupeaux contaminés n’aient pas été conservés vivants pour étudier l’évolution de la maladie et l’immunisation naturelle des animaux. La maladie semble bénigne : aucun animal n’est décédé. Il s’élève contre l’abattage total qui, selon lui, n’est pas pratiqué en Italie. Il demande la transparence sur le transport des carcasses et espère que celles-ci ne sont pas transportées dans d’autres régions encore indemnes de la maladie. D’après lui, on a compris que la maladie ne se transmet pas par contact direct entre animaux mais uniquement par un insecte piqueur. L’abattage total n’est pas exigé par les textes de l’UE.
La limite à l’abattage total ne serait-elle pas la capacité d’incinération des carcasses ?
En 2024, lors de la flambée épidémique de fièvre catarrhale ovine (FCO), les usines d’équarrissage avaient été saturées. Cette fragilité de la filière est reconnue par les autorités. L’équarrissage, un système fragile en cas de crise 2023 et Équarrissage, crises sanitaires et canicules : attention danger, Jeudi 09/05/2024. [16]
Les capacités réelles d’incinération proches de la Savoie et de la Haute Savoie sont-elles saturées ?
D’après les règlements européens règlement (CE) 1069/2009, les carcasses contaminées doivent être éliminées par incinération dans une usine agrée ou par enfouissement ou combustion sur place (exceptionnel). Les usines d’incinération proche de la Savoie sont situées dans l’Ain (Vonnas, usine Akiolis; Saint-Vulbas, Saria) ou l’Isère, Drôme (entreprise Saria).
Dans un enregistrement posté sur X (ex-Twitter [17]) le 6 août, Amélie Rebière, de la CR19, vice-présidente de la Coordination Rurale, interpelle directement la DRAAF (Direction régionale de l’alimentation, de l’agriculture et de la forêt) de Nouvelle-Aquitaine.
À la suite d’une interrogation, la société SOPA, équarrisseur du Cantal confirme le transport de 2 carcasses de Savoie vers le Cantal. La responsable de la DRAAF confirme que « le risque zéro n’existe pas » mais qu’il est très faible concernant la possibilité de diffusion de la maladie : les stomoxes (un des insectes vecteurs) ne piquent pas les animaux morts ; « le seul mode de transmission démontré scientifiquement serait l’insémination artificielle ».
Pourtant les experts s’accordent sur une transmission principale par insectes vecteurs. Il faut aussi rappeler que le virus de la DNC est assez résistant. En novlangue, transport de carcasse dans une autre région se dit « délestage » et abattage total se dit « dépeuplement ».
La réponse du Ministère a été ambigüe et incomplète « Non, les bovins abattus en Savoie à cause de la dermatose ne partent pas dans le Cantal pour y être incinérés » [18]
Des vaches de Haute-Loire sont en estivage en Savoie : que se passera-t-il au retour de ces animaux ? [19]
Conclusion
Les règlements européens (UE) semblent contradictoires et les experts ne semblent pas préconiser l’abattage des animaux sains. La surveillance clinique des troupeaux et le contrôle strict des mouvements d’animaux vivants associées à la vaccination seraient donc le moyen de contrôler la maladie.
La vaccination semble être la solution pour limiter les conséquences économiques de la dermatose nodulaire contagieuse (DNC) mais elle est incapable d’éradiquer la maladie, elle peut seulement la contenir. On ne connaît pas les conséquences à long terme de la recombinaison entre souches vaccinales et souches sauvages et le devenir de ces souches recombinantes qui semblent prendre le pas en Asie sur la souche sauvage (Banoun H et Lesgards JF, 2025).
Concernant la vaccination, il est crucial d’obtenir des données précises sur l’innocuité et l’efficacité des vaccins actuels, et de développer un vaccin plus protecteur sans pathogénicité résiduelle. Des recherches sont aussi nécessaires pour améliorer les modèles expérimentaux, mieux comprendre le rôle des petits ruminants et de la faune sauvage, et évaluer les risques liés à l’insémination artificielle et au transfert d’embryons.
La Confédération paysanne juge l’abattage total des troupeaux, même en cas de détection d’un seul animal infecté, comme une mesure disproportionnée, inefficace, et inhumaine. Ils estiment que cette pratique détruit non seulement des animaux sains, mais aussi le patrimoine génétique des élevages, représentant des décennies de travail, ainsi que l’identité et la viabilité économique des éleveurs.
La Confédération paysanne soutient activement les éleveurs qui s’opposent aux abattages, notamment par des blocages d’exploitations en Savoie et Haute-Savoie (ex. : ferme de la Mésange Bleue à Rumilly, GAEC Duchêne à Entrelacs).
Ces actions, menées avec la Coordination rurale, visent à empêcher l’euthanasie des troupeaux et à faire pression sur les autorités. Ils ont organisé des mobilisations, comme celle devant la préfecture de Chambéry le 24 juillet 2025, pour exiger un changement de politique sanitaire, et ont adressé des lettres ouvertes aux parlementaires, vétérinaires, scientifiques, et à la société civile pour fédérer un soutien plus large.
La France, leader européen en cheptel bovin, dépend fortement des exportations de bovins vivants et de produits transformés (viande, produits laitiers, cuirs). La DNC, classée comme maladie de catégorie A par l’Union européenne, impose des restrictions commerciales strictes si le « statut indemne » est perdu. L’abattage total vise à éradiquer rapidement la maladie pour maintenir l’accès aux marchés internationaux, notamment l’Italie, la Turquie, l’Algérie, et la Chine, qui sont sensibles aux crises sanitaires. Une perte prolongée de ce statut pourrait entraîner des pertes économiques massives pour la filière bovine, estimée à plusieurs milliards d’euros annuels.
La dermatose nodulaire contagieuse (DNC) entraîne donc de lourdes pertes économiques pour les éleveurs (perte de revenus, coûts sanitaires, difficulté à reconstituer les troupeaux) et un impact psychologique important, nécessitant un soutien étatique (indemnisations, accompagnement).
Les coûts indirects incluent la vaccination obligatoire, la désinfection et l’élimination des cadavres. En l’absence de mesures efficaces, la DNC pourrait s’étendre et compromettre les exportations. Une mauvaise gestion, à l’image de la fièvre Catarrhale Ovine (FCO), pourrait engendrer une crise structurelle durable. L’exportation de bovins vivants, essentielle à l’équilibre économique, reste très vulnérable aux crises sanitaires.
Le développement des produits transformés présente un potentiel à l’export, notamment en Asie, mais exige des investissements. La DNC représente un risque majeur pour la filière bovine française à court et long terme. Une stratégie sanitaire équilibrée, associant vaccination ciblée et indemnisations rapides, est essentielle pour préserver la compétitivité du secteur. Et aussi, une gestion humaine : « On peut juger la grandeur et la valeur morale d’une nation à la façon dont elle traite ses animaux. » affirmait Gandhi !
L’abattage total, ou dépeuplement, n’est pas rendu obligatoire par l’UE, c’est un choix du gouvernement français !
Comme énoncé dans ce rapport, il n’est pas éthique de ne pas soigner les bovins malades avec les traitements connus (publiés dans des revues scientifiques peer-reviewed) pour sauver le bétail de cette maladie, au lieu de le détruire, en parallèle des campagnes de vaccination des animaux dénués du virus.
Les sites à consulter
Suivi de l’épidémie et impact sur les troupeaux
Infos générales cheptel
https://www.agreste.agriculture.gouv.fr/agreste-web/disaron/SynAbo25440/detail/
Références
Références scientifiques
- Akther M, Akter SH, Sarker S, Aleri JW, Annandale H, Abraham S, Uddin JM. Global Burden of Lumpy Skin Disease, Outbreaks, and Future Challenges. Viruses. 2023 Aug 31;15(9):1861. https://pubmed.ncbi.nlm.nih.gov/37766268/
- ANSES 2017 Risque d’introduction de la dermatose nodulaire contagieuse en France, Avis de l’Anses, Rapport d’expertise collective, Juin 2017, Édition scientifique, Version révisée du rapport de février 2017 https://www.anses.fr/fr/system/files/SABA2016SA0120Ra.pdf
- Asset UK. Department for Environment, Food and Rural Affairs, UK, Updated Outbreak Assessment #4 Lumpy Skin Disease in North Africa 15 May 2025 Disease Report Rapport épidémiologique sur la dermatose nodulaire IV: collecte et analyse des données. https://assets.publishing.service.gov.uk/media/6830748d7fb7a7d9cd77528e/LSD_in_N_Africa__4_-_May_2025.pdf
- Banoun H et Lesgards JF. Le point sur la dermatose nodulaire des vaches en France en 2025 : la maladie, l’abattage, la vaccination, Researchgate, août 2025. https://www.researchgate.net/publication/394194310_Le_point_sur_la_dermatose_nodulaire_des_vaches_en_France_en_2025_la_maladie_l’abattage_la_vaccination
- Bhakha, K.; Matsui, Y.; Buakhao, N.; Wanganurakkul, S.; Deemagarn, T.; Oba, M.; Takemae, H.; Mizutani, T.; Misawa, N.; Chintapitaksakul, L.; et al. Development of a Multi-Locus Real-Time PCR with a High-Resolution Melting Assay to Differentiate Wild-Type, Asian Recombinant, and Vaccine Strains of Lumpy Skin Disease Virus. Vet. Sci. 2025, 12, 213. https://www.mdpi.com/2306-7381/12/3/213
- Bonaccorsi A, Garattini S, Jori A. Neurological Complications Of Smallpox Vaccination. Br Med J. 1964 Nov 28;2(5421):1345-7. Doi: https://doi.org/10.1136/bmj.2.5421.1345
- CNOPSAV 2025. Dermatose nodulaire contagieuse (DNC) : FNSEA / JA / FNB / FNPL / CDAF / LCA actent les décisions prises par l’Etat devant les membres du CNOPSAV Animal face à cette épizootie, Comité national d’orientation de la politique sanitaire animale et végétale, 17 juillet 2025, https://agriculture.gouv.fr/dermatose-nodulaire-contagieuse-bovine-dnc-les-acteurs-du-sanitaire-approuvent-la-strategie-de
- COUR DES COMPTES. 22.05.2023. Les soutiens publics aux éleveurs de bovins https://www.ccomptes.fr/fr/publications/les-soutiens-publics-aux-eleveurs-de-bovins
- Datten, B., Chaudhary, A.A., Sharma, S., Singh, L., Rawat, K.D., Ashraf, M.S., Alneghery, L.M., Aladwani, M.O., Rudayni, H.A., Dayal, D., Kumar, S. and Chaubey, K.K. Extensive examination of the significance, symptoms, diagnosis, available therapies, and prognosis of lumpy skin disease. Viruses 15(3), 604. https://pubmed.ncbi.nlm.nih.gov/36992313/
- DNC GDS Rhône. https://www.frgdsaura.fr/assets/uploads/GDS69/Bovins/Réu DNC 28-07-25 diapo avec commentaires.pdf
- EFSA 2016 : Urgent advice on lumpy skin disease EFSA Panel on Animal Health and Welfare, EFSA Journal, 29 July 2016, doi: 10.2903/j.efsa.2016.4573 https://efsa.onlinelibrary.wiley.com/doi/epdf/10.2903/j.efsa.2016.4573
- EFSA 2020 (European Food Safety Authority), Calistri P, De Clercq K, Gubbins S, Klement E, Stegeman A, Cortiñas Abrahantes J, Marojevic D, Antoniou SE and Broglia A, 2020. Scientific report on the lumpy skin disease epidemiological report IV: data collection and analysis. EFSA Journal 2020;18(2):6010, 36 pp. https://pubmed.ncbi.nlm.nih.gov/32874220/
- EFSA 2024 : Epizootie de dermatose nodulaire contagieuse bovine en Afrique du Nord, 5 novembre 2024, consulté le 3 août 2025, https://www.plateforme-esa.fr/fr/epizootie-de-dermatose-nodulaire-contagieuse-bovine-en-afrique-du-nord
- Eom HJ, Lee ES, Yoo HS. Lumpy skin disease as an emerging infectious disease. J Vet Sci. 2023 May;24(3):e42. https://pubmed.ncbi.nlm.nih.gov/37271510/
- Feyisa, A.F., 2018. A case report on clinical management of lumpy skin disease in bull. Vet. Sci. Technol., 9(3). https://www.researchgate.net/publication/326873550_A_Case_Report_on_Clinical_Management_of_Lumpy_Skin_Disease_in_Bull
- FLI (Friedrich-Loeffler-Institut). Carte : Foyers de la LSD depuis le 01.01.2025, situation au 31.07.2025 https://www.fli.de/de/aktuelles/tierseuchengeschehen/lumpy-skin-disease/ (https://www.fli.de/en/ news/animal-disease-situation/lumpy-skin-disease/)
- Gautam, M., P. Kattel and K. Kaphle. Review on lumpy skin disease and its emerging threat to livestock in Nepal. Veterinary Sciences: Research and Reviews, 8(1): 43-51. https://www.researcherslinks.com/current-issues/Review-Lumpy-Skin-Disease-Emerging-Threat-Livestock-Nepal/18/8/4966/html
- Garrow R P. FATALITY RATES OF SMALL-POX IN THE VACCINATED AND UNVACCINATED Br Med J 1928; 1:74. doi: https://doi.org/10.1136/bmj.1.3497.74
- Haegeman A, Sohier C, Mostin L, De Leeuw I, Van Campe W, Philips W, De Regge N, De Clercq K. Evidence of Lumpy Skin Disease Virus Transmission from Subclinically Infected Cattle by Stomoxys calcitrans. Viruses. 2023 May 30;15(6):1285. https://pubmed.ncbi.nlm.nih.gov/37376585/
- Haegeman A, De Leeuw I, Philips W, De Regge N. Development and Validation of a New DIVA Real-Time PCR Allowing to Differentiate Wild-Type Lumpy Skin Disease Virus Strains, Including the Asian Recombinant Strains, from Neethling-Based Vaccine Strains. 2023 Mar 28;15(4):870. https://pubmed.ncbi.nlm.nih.gov/37112850/
- Halder, B., & Seikh, B. (2022). Successful Management of Lumpy Skin Disease in Calf: A Case Study. Journal of Fisheries and Livestock Production, 10(2), 329. https://www.omicsonline.org/open-access/successful-management-of-lumpy-skin-disease-in-calf-a-case-study-119123.html
- Hidayatik N, Khairullah AR, Yuliani MGA, Hestianah EP, Novianti AN, Damayanti AN, Hisyam MAM, Moses IB, Ahmad RZ, Wardhani BWK, Wibowo S, Kurniasih DAA. Lumpy skin disease: A growing threat to the global livestock industry. Open Vet J. 2025 Feb;15(2):541-555. https://pubmed.ncbi.nlm.nih.gov/40201838/
- Hunter P, Wallace D. Lumpy skin disease in southern Africa: a review of the disease and aspects of control. J S Afr Vet Assoc. 2001 Jun;72(2):68-71. https://pubmed.ncbi.nlm.nih.gov/11513262/
- Kumar, N., Chander, Y., Kumar, R., Khandelwal, N., Riyesh, T., Chaudhary, K., Shanmugasundaram, K., Kumar, S., Kumar, A., Gupta, M.K., Pal, Y., Barua, S. and Tripathi, B.N. 2021. Isolation and characterization of lumpy skin disease virus from cattle in India. PLoS One 16(1), e0241022. https://pubmed.ncbi.nlm.nih.gov/33428633/
- Kumar N, Sharma S, Tripathi BN. Pathogenicity and virulence of lumpy skin disease virus: A comprehensive update. Virulence. 2025 Dec;16(1):2495108. https://pmc.ncbi.nlm.nih.gov/articles/PMC12036493/
- Le Monde, 23 mai 2023. https://www.lemonde.fr/planete/article/2023/05/23/la-cour-des-comptes-preconise-de-reduire-le-nombre-de-bovins-pour-tenir-les-engagements-climatiques-nationaux_6174548_3244.html
- Liang et al. Understanding the research advances on lumpy skin disease: A comprehensive literature review of experimental evidence. Front. Microbiol., 28 November 2022. Sec. Virology. Volume 13 – 2022 | https://doi.org/10.3389/fmicb.2022.1065894
- Mazloum, A., Van Schalkwyk, A., Babiuk, S., Venter, E., Wallace, D.B. and Sprygin, A. 2023. Lumpy skin disease: history, current understanding, and research gaps in the context of recent geographic expansion. Front. Microbiol. 14(1), 1266759. https://pubmed.ncbi.nlm.nih.gov/38029115/
- Mulatu, E., and Feyisa, A., Review: Lumpy skin disease. J. Vet. Sci. Technol., 9(3). https://doi.org/10.4172/2157-7579.1000535 https://www.researchgate.net/publication/326870960_Review_Lumpy_Skin_Disease
- Murti, N.T., Safitri, E., Srianto, P., Madyawati, S.P. and Rofikoh, A.R. Prevalence and progression of lumpy skin disease in cattle over six months leading up to Eid al-Adha in 2023 in the Cirebon District of West Java Province, Indonesia. IOP Conf. Ser. Earth Environ. Sci. 1292(1), 012037. https://iopscience.iop.org/article/10.1088/1755-1315/1292/1/012037
- OMSA-WHOA, dermatose nodulaire contagieuse, mise à jour du 22 juillet 2025, https://www.woah.org/fr/maladie/dermatose-nodulaire-contagieuse/
- Pandey, N., Hopker, A., Prajapati, G., Rahangdale, N., Gore, K. and Sargison, N. Observations of presumptive lumpy skin disease in native cattle and Asian water buffaloes around the tiger reserves of the central Indian highlands. N. Z. Vet. J. 70(2), 101–108. https://pubmed.ncbi.nlm.nih.gov/34546831/
- Paul, A.K., 2020. Management and treatment of lumpy skin disease in cattle at the Mohadevpur Upazila of Naogaon district of Bangladesh pp. 56. https://www.researchgate.net/publication/341072792_Management_ and_treatment_of_Lumpy_Skin_Disease_ in_cattle_at_the_Mohadevpur_upazila_of_ Naogaon_district_of_Bangladesh
- Samuelsson C, Hausmann J, Lauterbach H, Schmidt M, Akira S, Wagner H, Chaplin P, Suter M, O’Keeffe M, Hochrein H. Survival of lethal poxvirus infection in mice depends on TLR9, and therapeutic vaccination provides protection. J Clin Invest. 2008 May;118(5):1776-84. https://pmc.ncbi.nlm.nih.gov/articles/PMC2289795/
- Sanz-Bernardo B, Suckoo R, Haga IR, Wijesiriwardana N, Harvey A, Basu S, Larner W, Rooney S, Sy V, Langlands Z, Denison E, Sanders C, Atkinson J, Batten C, Alphey L, Darpel KE, Gubbins S, Beard PM. The Acquisition and Retention of Lumpy Skin Disease Virus by Blood-Feeding Insects Is Influenced by the Source of Virus, the Insect Body Part, and the Time since Feeding. J Virol. 2022 Aug 10;96(15):e0075122. https://doi.org/10.1128/jvi.00751-22
- Showler, A. T., & Osbrink, W. L. (2015). Stable Fly, Stomoxys calcitrans (L.), Dispersal and Governing Factors. International journal of insect science, 7, 19–25. https://pubmed.ncbi.nlm.nih.gov/26816486/
- Shridhar NB. LUMPY SKIN DISEASE : AN UPDATE ON TREATMENT AND VACCINATION BY DR N B SHRIDHAR, August 2022, DOI: 13140/RG.2.2.36513.89443
- Smriti S, Upasana V, Chitralekha D, Seema, Surendra KK and Ritu G. Successful therapeutic management of lumpy skin disease. The Pharma Innovation Journal. 2023; 12(8S): 467-469. https://www.thepharmajournal.com/special-issue?year=2023&vol=12&issue=8S&ArticleId=22106
- Standing Group of Experts on Lumpy Skin Disease in Europe under the GF-TADs umbrella (Global Framework for the Progressive Control of Transboudary Animal Diseases – OIE), First meeting (LSD1), Brussels, Belgium, 4-5 July 2016, et FAO, Hungary, Regional workshop on lumpy skin disease prevention, control, and awareness Budapest, Hungary, 7-9 March 2017 https://openknowledge.fao.org/items/16f89c10-f7c7-4e85-8e36-c7323125d7c1
- Tuppurainen E.S.M., Oura C.A.L. Review: Lumpy Skin Disease: An Emerging Threat to Europe, the Middle East and Asia. Transbound. Emerg. Dis. 2012;59:40–48. https://pubmed.ncbi.nlm.nih.gov/21749675/
- Tuppurainen E and Galon N. Lumpy skin disease: current situation in Europe and neighbouring regions and necessary control measures to halt the spread in south-east Europe, WHOA-OMSA, 2016. https://doc.woah.org/dyn/portal/index.xhtml?page=alo&aloId=34072
- Tuppurainen ESM, Antoniou SE, Tsiamadis E, Topkaridou M, Labus T, Debeljak Z, Plavšić B, Miteva A, Alexandrov T, Pite L, Boci J, Marojevic D, Kondratenko V, Atanasov Z, Murati B, Acinger-Rogic Z, Kohnle L, Calistri P, Broglia A. Field observations and experiences gained from the implementation of control measures against lumpy skin disease in South-East Europe between 2015 and 2017. Prev Vet Med. 2020 Aug;181:104600. https://pubmed.ncbi.nlm.nih.gov/30581092/
- Tuppurainen E, Dietze K, Wolff J, Bergmann H, Beltran-Alcrudo D, Fahrion A, Lamien CE, Busch F, Sauter-Louis C, Conraths FJ, De Clercq K, Hoffmann B, Knauf S. Review: Vaccines and Vaccination against Lumpy Skin Disease. Vaccines (Basel). 2021 Oct 6;9(10):1136. https://pubmed.ncbi.nlm.nih.gov/34696244/
- UE 2012. DÉCISION D’EXÉCUTION DE LA COMMISSION du 27 novembre 2012 modifiant les annexes I et II de la directive 82/894/CEE du Conseil concernant la notification des maladies des animaux dans la Communauté https://eur-lex.europa.eu/legal-content/EN/TXT/?uri=CELEX%3A32012D0737
- UE 2016. RÈGLEMENT (UE) 2016/429 DU PARLEMENT EUROPÉEN ET DU CONSEIL du 9 mars 2016 relatif aux maladies animales transmissibles et modifiant et abrogeant certains actes dans le domaine de la santé animale («législation sur la santé animale») https://eur-lex.europa.eu/legal-content/FR/TXT/?uri=celex%3A32016R0429
- UE 2018. https://eur-lex.europa.eu/legal-content/FR/TXT/?uri=CELEX:32018R1882
-
UE, Webinar on PPR and LSD in Europe under the GF-TADs umbrella, Overview of PPR and LSD in the EU, and the EU support to EU MS and neighbouring countries, Online Meeting, 3rd July 2025, from 09:00 to 11:30 am (CET), https://rr-europe.woah.org/app/uploads/2025/08/GFTADs_PPR_LSD_EU_DG_SANTE.pdf
- Wolff J, Krstevski K, Beer M, Hoffmann B. Minimum Infective Dose of a Lumpy Skin Disease Virus Field Strain from North Macedonia. Viruses. 2020 Jul 16;12(7):768. https://pubmed.ncbi.nlm.nih.gov/32708708/
- Zeynalova, S., Asadov, K., Guliyev, F., Vatani, M. and Aliyev, V. Epizootology and molecular diagnosis of lumpy skin disease in livestock in Azerbaijan. Front. Microbiol. 7(1), 1022. https://pubmed.ncbi.nlm.nih.gov/27446057/
Notes de bas de page (autres références)
[1] https://gtvbfc.com/index.php/2025/07/28/dermatose-nodulaire-contagieuse-en-savoie-et-haute-savoie-point-de-situation/
[2] https://agriculture.gouv.fr/dermatose-nodulaire-contagieuse-des-bovins-dnc-point-de-situation-et-foire-aux-questions .
[3] https://eur-lex.europa.eu/legal-content/FR/TXT/?uri=CELEX:32018R1882
[4] https://eur-lex.europa.eu/legal-content/FR/TXT/?uri=celex%3A32016R0429
[5] https://ec.europa.eu/transparency/documents-register/detail?ref=C(2025)4588&lang=fr
[6] https://ec.europa.eu/transparency/documents-register/detail?ref=C(2025)5363&lang=fr
[7] https://eur-lex.europa.eu/legal-content/FR/TXT/?uri=OJ:L_202501318
[8] https://idele.fr/detail-article/chiffres-cles-bovins-2024-productions-lait-et-viande
[9] https://drive.google.com/file/d/1mJebkkBijMyKYN5sArERaZSqDoXJfJ4A/view
[10] https://x.com/Dn641608671/status/1950935452594139583
[11] https://www.cdc.gov/smallpox/vaccines/index.html
[12] https://patentscope.wipo.int/search/en/WO2009101604
https://pmc.ncbi.nlm.nih.gov/articles/PMC3579898/
[13] https://www.thepharmajournal.com/archives/2023/vol12issue8S/PartF/S-12-8-153-572.pdf
[14] https://www.omicsonline.org/open-access/successful-management-of-lumpy-skin-disease-in-calf-a-case-study.pdf
[15] https://www.izs.it/BENV_NEW/datiemappe.html
[16] L’équarrissage, un système fragile en cas de crise https://www.lafranceagricole.fr/elevage/article/842996/l-equarrissage-un-systeme-fragile-en-cas-de-crise
Equarrissage, crises sanitaires et canicules : attention danger https://www.pleinchamp.com/actualite/equarrissage-crises-sanitaires-et-canicules-attention-danger
[17] https://x.com/coordinationrur/status/1953073485284090045
[18] https://www.lamontagne.fr/aurillac-15000/economie/non-les-bovins-abattus-en-savoie-a-cause-de-la-dermatose-ne-partent-pas-dans-le-cantal-pour-y-etre-incineres_14729838/
[19] https://www.leprogres.fr/economie/2025/08/06/en-estive-dans-les-alpes-des-vaches-de-haute-loire-cernees-par-l-epizootie-de-dnc